Dušična kiselina (nitratna kiselina), HNO3 jako je korozivna i izrazito toksična kiselina.
Koncentrirana je dušična kiselina jako oksidirajuće sredstvo. U čistom je stanju opisujemo kao bezbojnu tekućinu, koja starenjem poprima pomalo žutu boju zbog akumuliranja dušikovih oksida.
Zbog reakcije na svjetlost, nitratna (dušična) kiselina se obično čuva u tamno smeđim bocama. Ako je u prozirnim bocama, izložena svjetlosti – može doći do reakcije fotolitičke razgradnje u dušikov tetroksid (N2O4).
Dušična kiselina poznata je po tome što otapa većinu metala. Prilikom otapanja metala nastaju odgovarajući nitrati. Osim toga što reagira sa metalima, koncentrirana dušična kiselina reagira sa nekim nemetalima, pa dolazi do reakcije kojom nastaje okso kiselina ili oksid.
Čista (nerazrijeđena – bezvodna) dušična kiselina na sobnoj temperaturi je bezbojna tekućina gustoće 1,522 g/cm³. Kiselina će se skrutiti na temperaturi od -42°C tvoreći bijele kristale. Temperatura vrelišta dušična kiseline je 83°C.
Ako je izložena izvoru svjetlosti, čak i pri sobnoj temperaturi, dolazi do djelomične razgradnje dušične kiseline, a kao produkt te kemijske reakcije nastaje dušikov dioksid opisan formulom ispod:
4 HNO3 → 2 H2O + 4 NO2 + O2 (72°C)
Zbog reakcija koje smo spomenuli u tekstu iznad, lako je zaključiti da se bezvodna dušična kiselina pravilno skladišti na temperaturi ispod 0°C da bi se izbjegla razgradnja. Dušikov dioksid (NO2) ostaje otopljen u dušičnoj kiselini i daje joj žutu boju. Za razliku od čiste kiseline iz koje izlaze bijele pare, kiselina s otopljenim NO2 ispušta crvenkasto-smeđe pare, zbog čega se često navodi kao “crvena dimeća kiselina” ili “dimeća dušična kiselina”.
Dimeća dušična kiselina se također navodi kao 16-molarna dušična kiselina, najkoncentriraniji oblik dušične kiseline pri standardnoj temperaturi i tlaku (0°C, 100 kPa).
U promet (za korištenje) se najčešće stavlja 68%-tna dušična kiselina. Ona se dobije destiliranjem manje koncentrirane dušične kieline.
Industrijska proizvodnja dušične kiseline

Dušična kiselina danas se proizvodi Ostwaldovim procesom, nazvanim po njemačkom kemičaru Wilhelmu Ostwaldu.
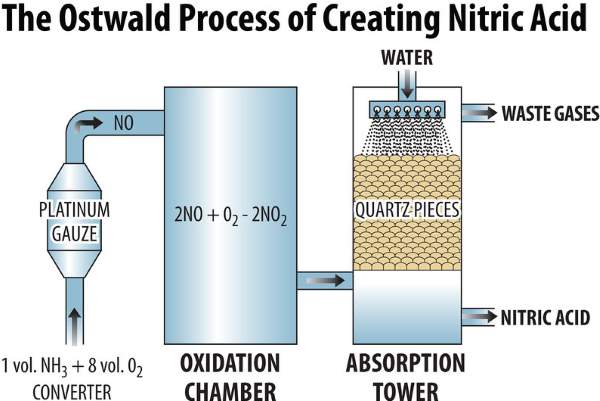
U ovom procesu bezvodni amonijak se oksidira u dušikov oksid, koji zatim reagira s kisikom iz zraka čime nastaje dušikov dioksid. On se dalje apsorbira u vodi, čime nastaje dušična kiselina i dušikov oksid.
Dušikov oksid se zatim vraća u proces, da bi se izdvojila što veća količina dušične kiseline. Na donjoj fotografiji možete pogledati skicu – Ostwaldov postupak proizvodnje dušične, odnosno nitratne kiseline.
Moguće je dušičnu kiselinu dobiti u laboratoriju, posebnim kemijskim reakcijama. O tome ćemo pisati u nastavku, pa ćemo spomenuti i uporabu dušične kiseline, kao i sigurnost pri rukovanju.
Ukratko – : Nitratna kiselina, HNO3, jedna od najjačih mineralnih kiselina. Prepoznajemo je kao bezbojnu tekućinu koja se na zraku dimi, a na svjetlu postaje žuta i rastvara se stvarajući dušični dioksid (NO2).
Možemo kazati da je dušična kiselina jedan od najvažnijih anorganskih spojeva. Otapa gotovo sve kovine, osim zlata (ali u kombinaciji sa kloridnom kiselinom otapa i zlato), platine i iridija, stvarajući nitrate. Jako oksidacijsko sredstvo pa se upotrebljava u mnogim kemijskim procesima.
Dobiva se iz čilske salitre djelovanjem sulfatne kiseline (nitratni postupak). Može se dobiti spajanjem atmosferskog dušika i kisika u električnom luku.
Kao smjesa sa sulfatnom kiselinom upotrebljava se za nitriranje organskih tvari, odnosno za priređivanje spojeva koji služe u proizvodnji plastičnih masa, boja, eksploziva i spojeva važnih u poljoprivredi.
Laboratorijska sinteza – Dobivanje dušične kiseline u laboratoriju
Dušična kiselina može se dobiti u laboratoriju. Potrebno je potaknuti kemijske reakcije s otprilike jednakim udjelima (masenim) nitratne soli (npr. bakrov(II) nitrat) i 96% sulfatne kiseline (H2SO4) i zatim destilacijom smjese na temperaturi vrelišta dušične kiseline od 83°C sve dok bijela kristalna masa (metalni sulfat) ne zaostane u reakcijskoj posudi. Kemijska reakcija napisana je u nastavku.
H2SO4 + NO3– → HSO4– (s) + HNO3 (g)
Dobivena crvena dimeća dušična kiselina može se naknadno prevesti u bijelu dušičnu kiselinu.
Uporaba dušične kiseline
Danas smo našli mnoge primjene dušične kiseline, no prednjači uporaba u proizvodnji umjetnih gnojiva. Trenutno se najviše koristi u poljoprivredi (poljoprivrednim preparatima).
Svakako treba spomenuti veliku primjenu dušične kiseline u proizvodnji eksploziva, posebno rudarskog eksploziva i eksploziva za vojnu primjenu.
Dušična kiselina se koristi za graviranje i otapanje metala, u kemijskoj sintezi, proizvodnji pića, proizvodnji stakla i raznih sredstava za čišćenje.
Mnogima je danas zanimljiva dušična kiselina kao sastavni dio smjese kiselina koje tvore zlatotopku (aqua regia – koja otapa zlato). U modernom dobu sve je više zastupljeno recikliranje zlata iz elektroničkog otpada, a tu će najbolje poslužiti zlatotopka.
Sigurnost pri rukovanju
Rukovanje kiselinama uvijek zahtjeva oprez, a uvjeti za rad trebaju biti odgovarajući. Mjere opreza vrijede i u ovom slučaju, posebno jer je dušična kiselina jako oksidirajuće sredstvo, sa otrovnim isparavanjima i potencijalnim eksplozivnim reakcijama.
Važno je spomenuti da dušična kiselina može snažno reagirati sa spojevima kao što su cijanidi, karbidi i metalni prah, te da može doći čak i do eksplozije.


